宿主细胞蛋白(HCPs)是生物治疗药物中与工艺相关的关键杂质,会影响药物的稳定性和安全性。治疗性蛋白与残留HCPs成分的动态范围极大,往往大于5个数量级,导致高风险HCPs检测更加困难。LC-MS/MS检测可以突破传统免疫分析方法在灵敏度和特异性方面的局限性,已成为有效检测和定量HCPs的关键工具,可指导下游纯化工艺并监测HCPs清除效果。
2025年6月,中国医学科学院北京协和医学院的张金兰教授课题组在Journal of Proteome Research发表了一套新的HCPs监测方法,首先通过数据依赖采集(DDA)构建包含所有潜在HCPs的CHO细胞蛋白库,然后对38种已报道的高风险HCPs进行了平行反应监测(PRM)和多重反应监测(MRM)交叉验证,最终筛选出28种高风险HCPs及其特异性肽段和离子对信息。下一步建立并验证了一种新的动态MRM(dMRM)方法,可以同时定量28种高风险HCPs。最后,应用上述策略分析了五个纯化的单克隆抗体制备工艺样品,通过DDA方法对未知HCPs进行全面分析,使用dMRM方法对28种已知高风险HCPs进行快速定量。总体而言,该策略能够对已知和未知HCPs进行全面分析,指导生物制药工艺的优化。本研究中DDA数据分析使用PEAKS Studio完成。
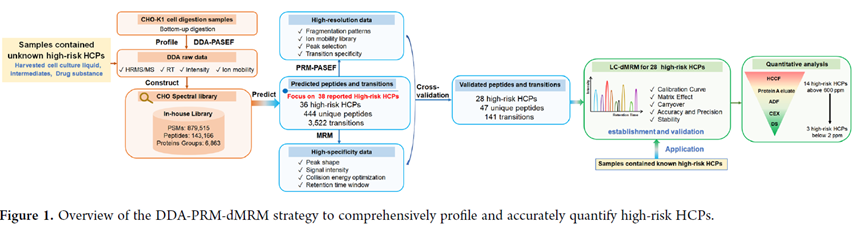
该项研究中整合了 DDA(全面分析已知和未知HCPs)、PRM(验证特异性)和 dMRM(快速定量已知高风险 HCPs)的不同方法,实现了HCPs的全面分析,为生物制药过程中HCPs的监测提供了高效、全面的解决方案,助力优化纯化工艺、提升药物质量可控性,符合QbD理念。但目前仅基于 CHO-K1 细胞系,可能无法覆盖其他 CHO 亚型或变异株的 HCPs,未来可扩展至其他宿主细胞系或微生物表达系统,结合人工智能和深度学习,扩展低丰度 HCPs的特征谱图数据,建立HCP谱图库共享平台。

