

Protein de novo sequencing and glycan profiling software
PEAKS®AB是一款基于高分辨LC-MS/MS数据联合正交酶解方法,实现对抗体/蛋白的全自动从头测序软件。
软件可精准分析翻译后修饰(PTM)与序列突变,实现糖基化位点全景表征,提供直观的手动核验与同源序列查找,一站式满足抗体/蛋白研究需求。
全自动蛋白测序解决方案
功能核心:
- 全自动化的抗体与蛋白从头测序
- 精准的异亮氨酸/亮氨酸(Ile/Leu)鉴别
- 抗体/蛋白序列的Peptide Mapping分析
- 深度的聚糖全景解析
- 翻译后修饰与序列变异的定量分析
- 支持手动编辑和查找同源序列
- 支持用户自定义结果报告形式
- 仪器厂商中立,支持Orbitrap、timsTOF、ZenoTOF数据
PEAKS AB 软件的自动化流程以及可编辑的人工核验模式可以进一步提高测序的准确性。它还提供了一个更加方便和用户友好的工作流程,用于抗体测序分析,并且可以为用户提供新的定制功能。
软件概览
抗体与蛋白完整序列从头测序
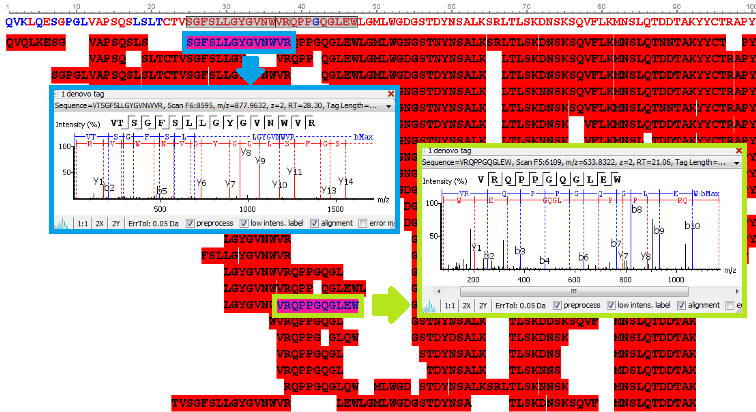
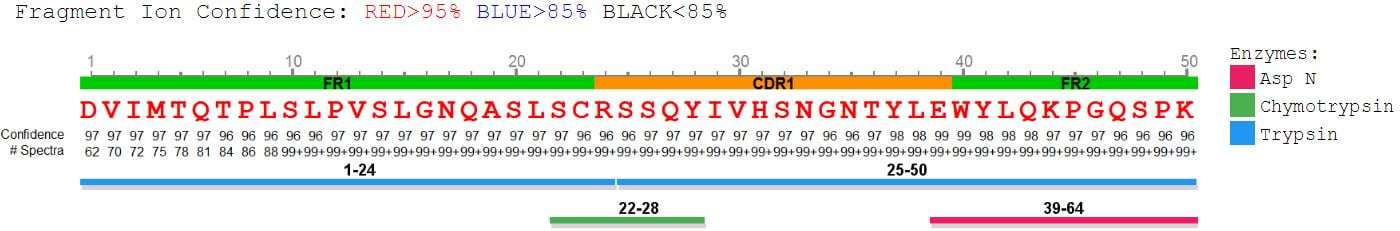
基于碎片离子提供的直接证据生成高可信度从头测序序列标签,经肽段de novo测序后,无需参考序列,将其组装为完整的抗体/蛋白序列。点击肽段查看谱图,可直接在谱图上标注碎片离子对应的每一个氨基酸。
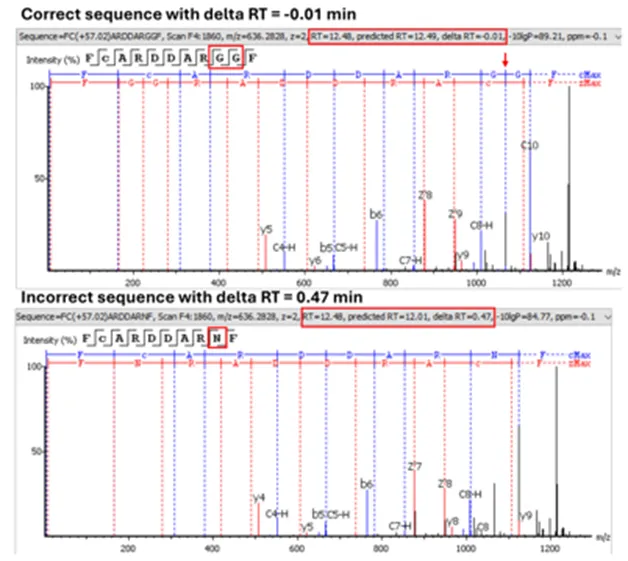
基于保留时间预测优化中等质量氨基酸区分,结合质谱碎片离子直接证据,确保测序的精准度。并在de novo结果中,展示预测保留时间和实测保留时间的差值帮助人工确证。
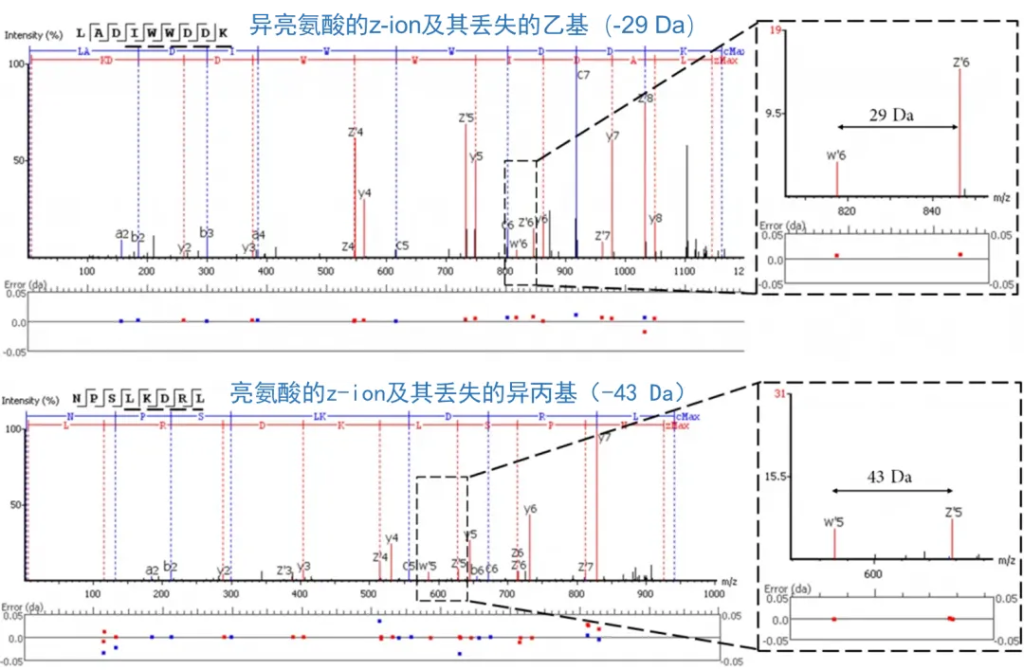
利用w-ion精准鉴别 Ile/Leu,填补传统测序的关键盲区。
丰富的交互式可视化展示,便于谱图校验
整合全序列信息,显示每个氨基酸来自碎片离子的直接证据。
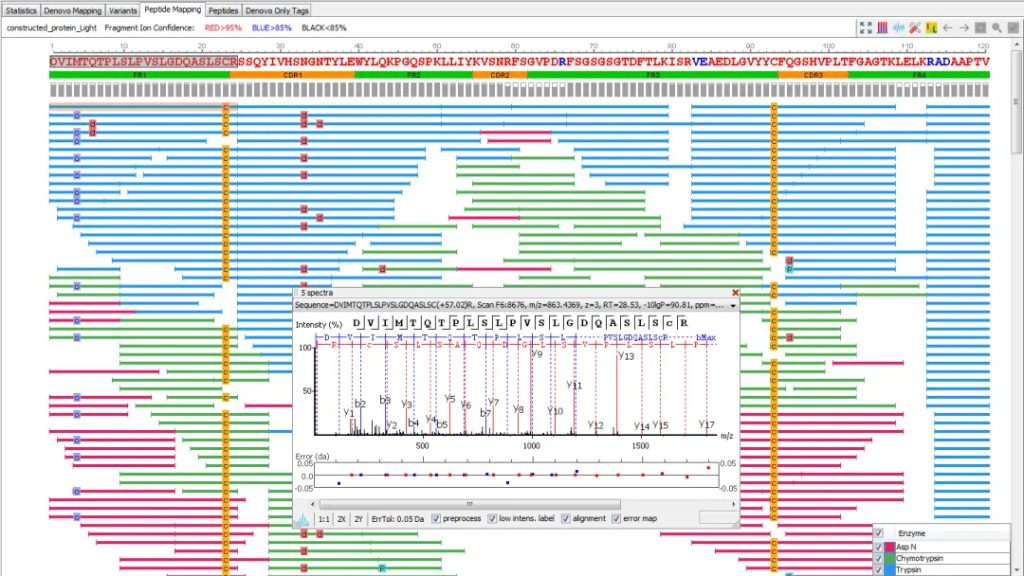
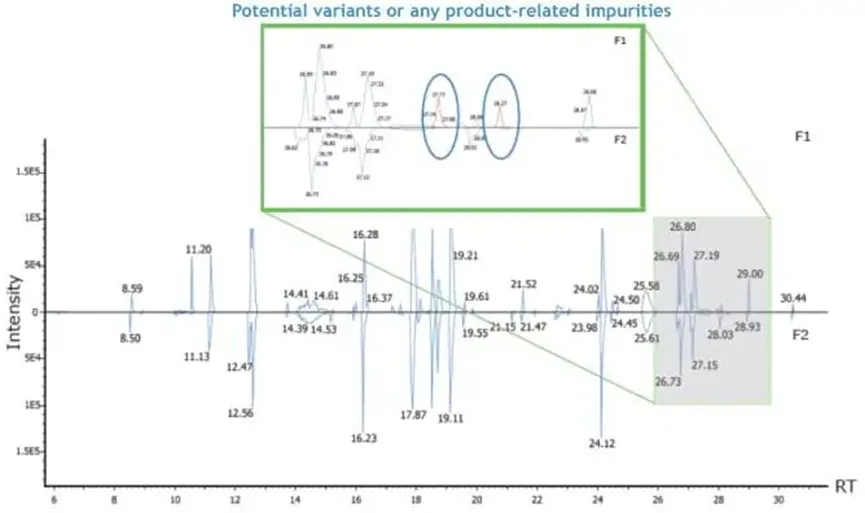
Peptide Mapping可自动对比、注释不同样品谱图信息,标明可能发生的序列突变,以便进行后续产品质控或其他任何相关研究(蓝色峰标注来自参考蛋白的肽段、红色峰高亮突变/杂质肽)。
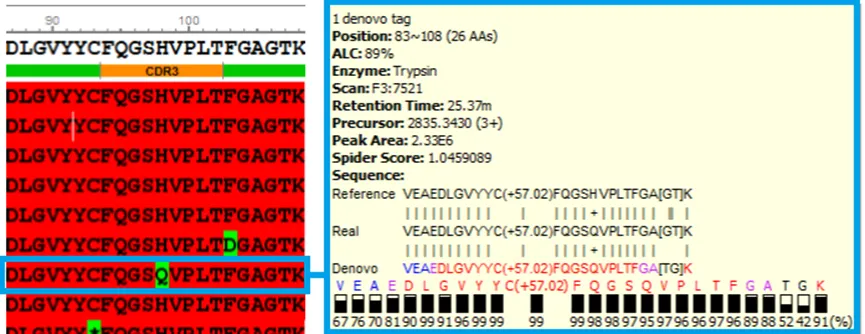
序列变异视图自动高亮标注转录错误导致的氨基酸变异、截短位点,直观可视化异常序列。
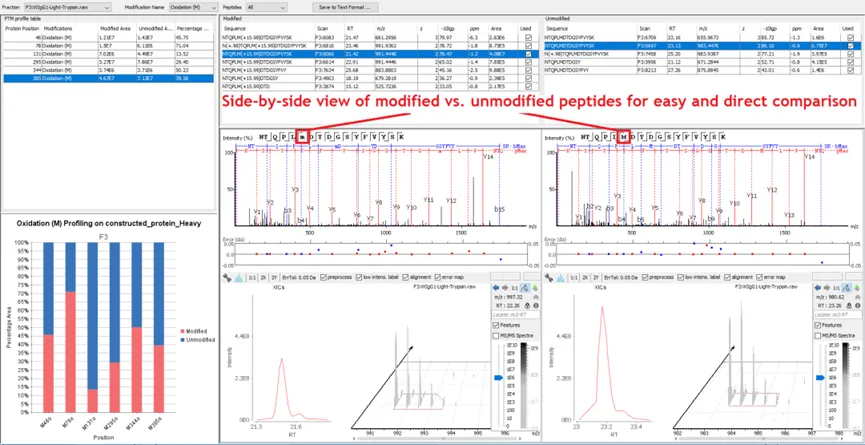
PTM Profiling清晰展示了含修饰位点的每一条序列的修饰/未修饰肽段谱图,并提供基于XIC的精准定量数据。
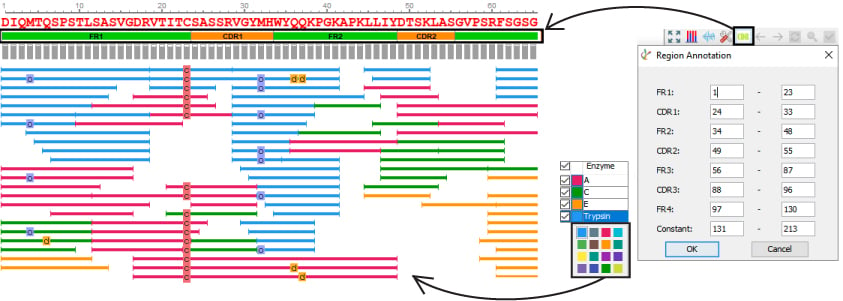
此外,在PTM功能模块中也可以对序列CDR功能区注释的设置和修改。
深度聚糖全景解析
内置Glycan Profiling工具,精准映射糖肽至抗体序列,解决糖肽-序列对应混乱、位点定位不准问题。按酶解产物分类分析聚糖谱,直观展示位点聚糖组成与相对丰度,并自动匹配N/O-linked糖库完成聚糖结构注释和准确的糖基化位点信息,一站式实现抗体糖基化定性定量分析。
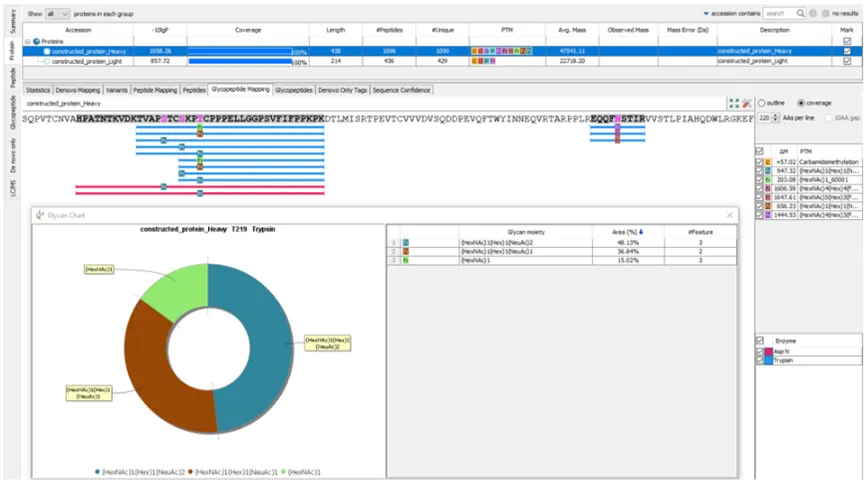
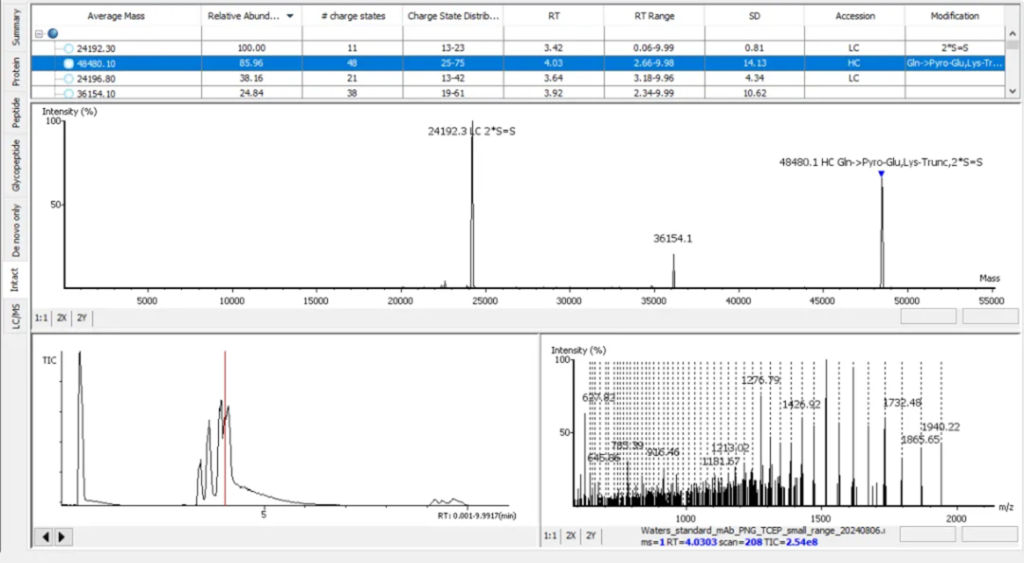
Intact Mass解析
软件利用完整分子量解卷积算法,得到准确的分子量。测量结果可以用于验证测序组装结果的准确性,并从N端,C端,糖基化修饰等角度来注释分子量的结果。
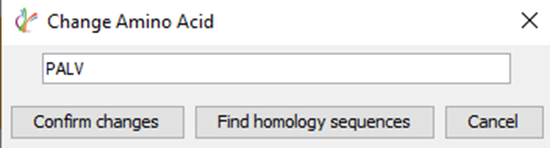
手动编辑和同源序列查找
软件为每个PSM赋予局部置信度(CAA)分数,为序列拼接过程中多肽的选择提供更可靠的确证;支持用户手动挑选代表性肽段,让序列拼接更精准、更可控。
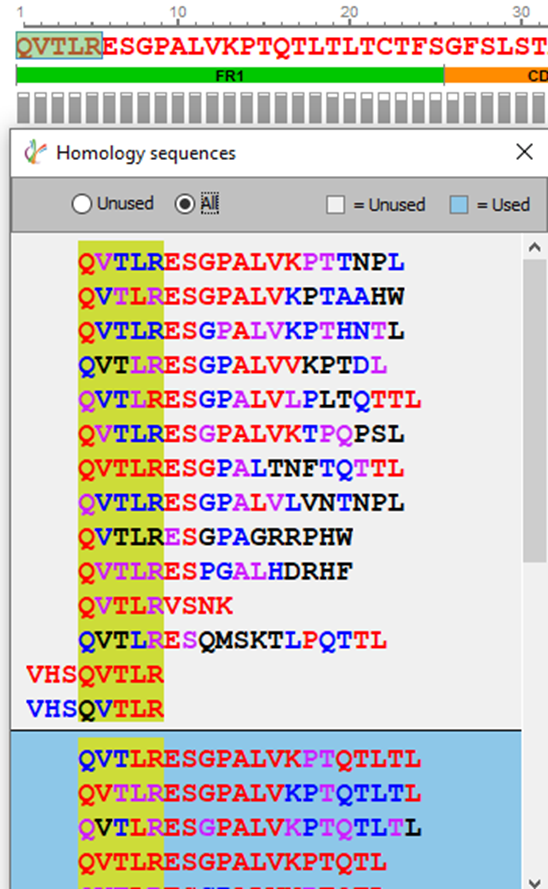
用户可通过选择3个或更多的氨基酸,在“查找同源序列”中显示任何可以映射到该区域的多肽序列用于同源序列替换。
备选多肽序列按氨基酸局部置信度评分进行颜色编码,快速评估结果质量。用户可以选择待编辑的氨基酸,修改序列并保存,将在第二轮序列组装后,生成一个新的测序结果节点。
算法
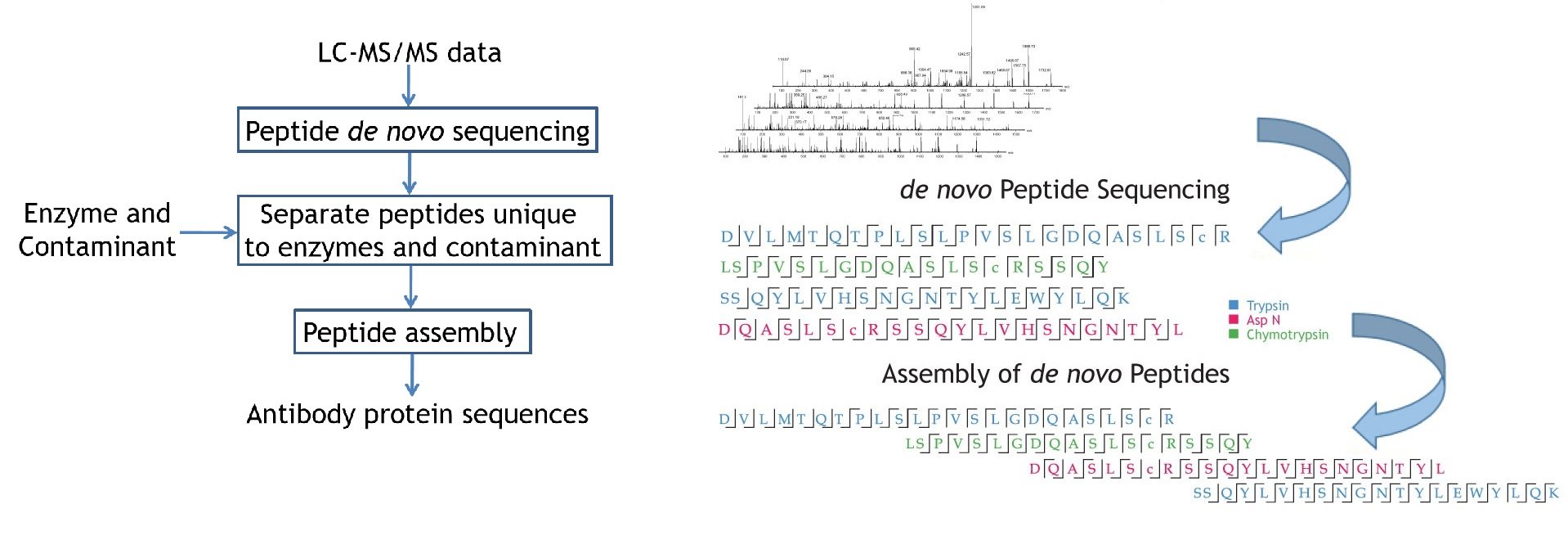
PEAKS®AB软件可以利用正交设计的多酶联合酶解的抗体/蛋白,通过高分辨率LC-MS/MS获得的数据集,直接对抗体/蛋白进行序列分析。
首先进行肽段的de novo sequencing,随后将可信度高的序列标签自动组装成抗体/蛋白序列。
报告生成
- 抗体样品描述
- 缩略词说明
- 实验流程
- 抗体轻/重链信息
- 氨基酸序列
- 蛋白/抗体序列全覆盖的peptide mapping
- 可视化覆盖可变区的代表型肽段
- 区分Ile/Leu
- 抗体轻链
- 氨基酸序列
- 蛋白/抗体序列全覆盖的peptide mapping
- 可视化覆盖可变区的代表型肽段
- 区分Ile/Leu
- 一键导出Glycan Profiling聚糖分析报告
References
- Shan, B. and Xin, L. Integrating de novo Sequencing and Database Search for Monoclonal Antibody Sequencing. J Biomol Tech. 24(Suppl). S62–S63. 1/5/2013.
- Tran, N.H. et al. Complete De Novo Assembly of Monoclonal Antibody Sequences. Scientific Reports. 6:31730. 26/08/2016.


